One Tube Mutagenesis Kit 一管式突变试剂盒
产品介绍:
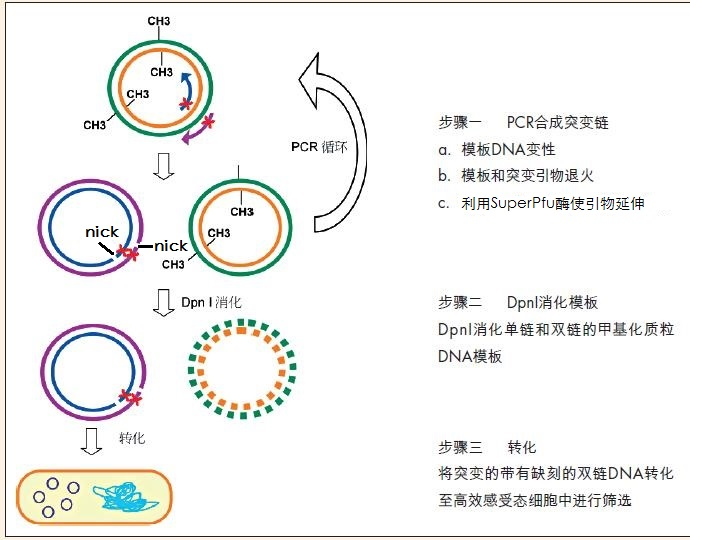
本定点突变试剂盒是基于PCR原理向目的DNA片段(一般为质粒)中引入碱基的点突变,多个邻近密码子的突变,单个或多个邻近密码子的缺失(deletion)或插入(insertion)等。一般宿主菌培养扩增的质粒DNA是甲基化的,PCR扩增新合成的DNA是非甲基化的。首先以待突变的甲基化质粒为模板,利用高保真的SuperPfu聚合酶实现突变质粒的合成(非甲基化,包含突变点,且有两个缺刻点nick点),再利用Dpn I酶选择性降解甲基化的模板质粒 ,剩下的新合成非甲基化的突变质粒转入大肠杆菌后,质粒中有两个nick位点可以被大肠杆菌修复,得到的克隆就会含有预期的突变质粒了。一般可以产生大于90%的突变效率。
产品储存:-20℃ 保存,有效期12个月。由于试剂盒中提供的反应缓冲液及dNTP等成份是为反应专门优化的,所以不要用其它的反应缓冲液及dNTP等代替。
适用范围:< 10kb甲基化质粒中核苷酸的突变。
 特点:
特点:简单,一个PCR管中完成所有操作;采用部分重叠引物设计,使PCR呈指数扩增,扩增产物凝胶电泳可见;使用Dpn I去除非突变模板,突变效率高达90%。
引物设计:
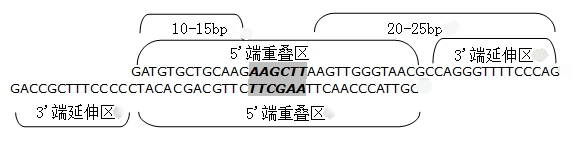
1、引物包含5'端重叠区和3'端延伸区。5'端重叠区长度大约25-30bp,3'端延伸区长度大约是10-15bp。
2、突变位点设计在5'端重叠区的中间位置,突变位点的左侧5'端大约10-15bp,右侧3'端20-25bp。
3、计算引物的Tm值,看是否达到78℃,如果Tm值低于78℃,则适当改变引物的长度以使其Tm值≥78℃。
定点突变Tm值计算公式:Tm=81.5+0.41×(%GC)–675/L-%mismatch
注:L:引物碱基数;%GC:引物GC含量百分数;%mismatch:突变位点数/引物长度数的百分数。
缺失或者插入Tm值计算公式:Tm=81.5+0.41×(%GC)–675/L
注:L:引物碱基数,不包括插入碱基或者缺失碱基数;%GC:引物GC含量百分数
4、引物应该选择PAGE或者更高的纯化方式,GC含量应大于40%,3'端为一个或者更多个G/C结尾。
5、举例:GCGATT连续突变前4个碱基成为AAGCTT(引入一个Hind III酶切位点)
突变前序列:CTGGCGAAAGGGGGATGTGCTGCAAG
GCGATTAAGTTGGGTAACGCCAGGGTTTTCCCAG
GACCGCTTTCCCCCTACACGACGTTC
CGCTAATTCAACCCATTGCGGTCCCAAAAGGGTC
设计突变引物:
建议PCR反应条件(以25μl为例):
|
Template
|
10-20ng
|
|
Forward Primer (10 μM)
|
1 μl
|
|
Reverse Primer (10 μM)
|
1 μl
|
|
10×SuperPfu Buffer
|
2.5 μl
|
|
10 mM dNTPs
|
1 μl
|
|
SuperPfu DNA Polymerase
|
0.5 μl
|
|
ddH2O to final
volume
|
25 μl
|
注意:如质粒大于4kb,dNTPs使用量为2μl
PCR循环:
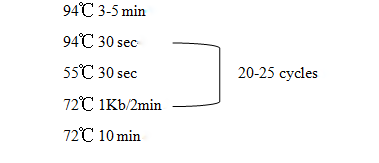 电泳检测:
电泳检测:
取5μl PCR产物,1% 琼脂糖凝胶电泳检测。如能看见目的条带,则已成功大半;注意即使未见条带或者见到目的条带外还有其它条带,也可以继续进行后续步骤。
PCR产物的消化:
直接加 0.5μl Dpn I酶于PCR产物中(约20μl),充分混匀,继续PCR仪器上37 ℃孵育1小时(不用热盖)。
注意:Dpn I含甘油,易沉底,一定要吹打混匀。如果非突变质粒较多,可以延长消化时间到3-5小时。
转化:
加入5-10μl Dpn I酶消化产物于50μl-100μl感受态细胞中(效率≥10的8次方),轻弹混匀,冰浴30 分钟。按照标准转化步骤转化,最后将菌液铺板,培养过夜(为得到较多的克隆,4000 rpm 离心1min,弃掉部分上清,保留100-150μl,轻弹悬浮菌体,取全部菌液涂板,培养过夜)。
注意:如无克隆生长,或克隆数少,把Dpn I酶消化后的产物用常规的乙醇沉淀浓缩,这样就可以把所有的产物全部用于转化。





